您现在的位置是: 首页 > 教育新闻 教育新闻
高考化学经典题目_化学高考经典例题
tamoadmin 2024-05-23 人已围观
简介忘的差不多了,我就按我说的,你自己考虑下!因为是完全燃烧,就是该烃与氧气的分子式比是一比五的。这是体积比决定 的。烃是C和H够成的,不知道有没有O。(忘 了)就是一个该烃要消耗5O2。完全燃烧的产物只有水H2O和CO2.假设该分子式是CXHY.就有X个CO2分子。Y/4个水分子。CxHy+(x+ y/4)O2 xCO2+ y/2H2O该通式可分解成①Cx+xO2xCO2和②Hy+y/4 O2y/2
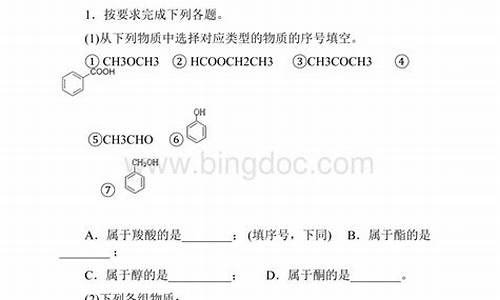
忘的差不多了,我就按我说的,你自己考虑下!因为是完全燃烧,就是该烃与氧气的分子式比是一比五的。这是体积比决定 的。烃是C和H够成的,不知道有没有O。(忘 了)就是一个该烃要消耗5O2。完全燃烧的产物只有水H2O和CO2.假设该分子式是CXHY.就有X个CO2分子。Y/4个水分子。CxHy+(x+ y/4)O2 xCO2+ y/2H2O
该通式可分解成①Cx+xO2→xCO2和②Hy+y/4 O2→y/2 H2O
当y=4时,反应前后体积不变;当y>4时,燃烧后体积增大;当y<4时,燃烧后体积减小。
二、1000C以上,烃的含氧衍生物燃烧通式:CxHyOz + (x+y/4-z/2) xCO2+y/2H2O。当y=4-2z时,燃烧前后体积不变;当y>4-2z时,燃烧前后体积增大;当y<4-2z时,无此含氧衍生物。
第一题:
这道题用化学解题的常用方法:极值法。氢气的体积在标况下为11.2L,那么求出氢气的物质的量n=V/Vm=11.2/22.4=0.5mol,氢气的质量:m=n·M=0.5*2=1g,根据列方程式计算,生成1g氢气需要32.5g锌,28g铁,9g铝和12g镁,想混合后质量是10g放出1g氢气前提就是一个质量比10g小,另一个质量比10g大,只有铝的质量比10g小,所以必须有的金属是铝。
第二题:
这道题主要考察的是金属与酸反应的方程式,但是特别要注意的一点是钠不仅能与酸反应放出氢气,还能与水反应放出氢气,这是本题的关键。盐酸的物质的量为n=c*V=1*0.1=0.1mol,题中给出金属的物质的量和酸的物质的量,这时我们应该注意:镁铝与酸反应时时过量的,所以算放出氢气体积的时候应该以酸的物质的量为依据:
Mg ~ 2HCl ~ H2 2Al ~ 6HCl ~ 3H2
1 2 1 2 6 3
0.05mol 0.1 mol 0.05mol 0.1/3mol 0.1 mol 0.05mol
钠因为与水反应也能放出氢气(2Na +2H2O =2NaOH +H2),所以这时我们在计算钠放出氢气时只考虑钠的物质的量就可以了:
2Na ~ H2
0.3mol 0.15mol
所以同温同压下产生气体的体积比为0.15:0.05:0.05=3:1:1









